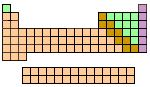Es el momento de aprender y conocer toda la información que nos aporta la TABLA PERIÓDICA. Tenemos 118 elementos, de los cuales 90 naturales, Este año, 2017, se han aprobado los nombres para los elementos de número atómico 113, 115, 117 y 118.
Los elementos químicos están ordenados en la Tabla Periódica en orden creciente de número atómico, y dispuestos en 18 grupos o familias (las columnas) y 7 períodos (las filas). Generalmente cada grupo contiene elementos con el mismo número de electrones de valencia (en la última capa), lo que hace que tengan propiedades muy semejantes.
Los grupos más conocidos tienen nombres característicos: alcalinos, alcalino-térreos, térreos (grupo del boro), anfígenos (grupos del oxígeno), halógenos (grupo del flúor), gases nobles, etc.
En el siguiente enlace tienes una amplia información de la tabla periódica: http://www.ptable.com/?lang=es
A16.- Fíjate en la tabla periódica del dibujo superior. Indica el período y el grupo de la tabla en que colocarías los siguientes elementos, sin mirar la tabla: Manganeso, Mn (Z= 25); hierro, Fe (Z= 26), cobre, Cu (Z= 29);Cinc, Zn (Z= 30); níquel, Ni (Z= 28); galio, Ga (Z= 31); germanio, Ge (Z= 32); arsénico, As (Z= 33); bromo, Br (Z= 35); kriptón, Kr (Z= 36); titanio, Ti (Z= 22); cromo, Cr (Z= 24).
A17.- Observa la forma de la tabla periódica y contesta:
a) ¿Por qué crees que tiene una forma tan extraña, en lugar de ser una figura regular rectangular? ¿Por qué crees que aparece ese hueco en la parte superior?
b) Las dos filas que colocamos fuera, ¿dónde se colocarían si estuvieran dentro de la tabla periódica?
c) ¿Por qué el hidrógeno aparece situado a la izquierda y en la misma columna que los elementos litio, sodio, etc? ¿Tienes propiedades de esos elementos?
Una de las características de la Tabla Periódica es que las propiedades de los elementos varían de forma periódica. De ellas, sólo vamos a estudiar el carácter metálico.
El carácter metálico está relacionado con las propiedades físicas y químicas de los elementos. Este carácter disminuye a medida que nos desplazamos hacia la derecha por un período, y aumenta dentro de un grupo, hacia abajo. Según esto podemos distinguir tres familias: metales, no metales y semimetales.
A18.- Los elementos metales se agrupan en las familias 1 al 12 en los grupos alcalinos, alcalino-térreos y metales de transición. Indica los principales elementos de estos grupos.
A19.- Los elementos no metales están en los grupos del 14 al 18. Indica los nombres de estos grupos y sus principales elementos?
A20.- Hay un grupo de elementos semimetales o metaloides, que están en los grupos 13 al 17, en medio de metales y no metales. ¿Cuáles son estos elementos?
A21.- ¿En qué lado de la Tabla Periódica es más acentuado el carácter metálico: derecho o izquierdo? ¿Y quién tendrá carácter más metálico, el potasio o el cinc?
A22.- Resume las características de cada familia, metales, no metales y semimetales.
A23.- Consulta la tabla periódica y clasifica los siguientes elementos en metales, no metales y semimetales: bario, yodo, cobalto, nitrógeno, hierro, hidrógeno, germanio, plomo, cromo, bromo, arsénico, azufre, rubidio, cadmio y uranio.
A24.- Los elementos artificiales son los de número atómico 43, 61 y 93 en adelante. Localiza en la tabla periódica los elementos 43, 61, 93, 94, 95. 103 y 106 e indica sus nombres y símbolos.
Los elementos químicos están ordenados en la Tabla Periódica en orden creciente de número atómico, y dispuestos en 18 grupos o familias (las columnas) y 7 períodos (las filas). Generalmente cada grupo contiene elementos con el mismo número de electrones de valencia (en la última capa), lo que hace que tengan propiedades muy semejantes.
Los grupos más conocidos tienen nombres característicos: alcalinos, alcalino-térreos, térreos (grupo del boro), anfígenos (grupos del oxígeno), halógenos (grupo del flúor), gases nobles, etc.
En el siguiente enlace tienes una amplia información de la tabla periódica: http://www.ptable.com/?lang=es
A16.- Fíjate en la tabla periódica del dibujo superior. Indica el período y el grupo de la tabla en que colocarías los siguientes elementos, sin mirar la tabla: Manganeso, Mn (Z= 25); hierro, Fe (Z= 26), cobre, Cu (Z= 29);Cinc, Zn (Z= 30); níquel, Ni (Z= 28); galio, Ga (Z= 31); germanio, Ge (Z= 32); arsénico, As (Z= 33); bromo, Br (Z= 35); kriptón, Kr (Z= 36); titanio, Ti (Z= 22); cromo, Cr (Z= 24).
A17.- Observa la forma de la tabla periódica y contesta:
a) ¿Por qué crees que tiene una forma tan extraña, en lugar de ser una figura regular rectangular? ¿Por qué crees que aparece ese hueco en la parte superior?
b) Las dos filas que colocamos fuera, ¿dónde se colocarían si estuvieran dentro de la tabla periódica?
c) ¿Por qué el hidrógeno aparece situado a la izquierda y en la misma columna que los elementos litio, sodio, etc? ¿Tienes propiedades de esos elementos?
Una de las características de la Tabla Periódica es que las propiedades de los elementos varían de forma periódica. De ellas, sólo vamos a estudiar el carácter metálico.
El carácter metálico está relacionado con las propiedades físicas y químicas de los elementos. Este carácter disminuye a medida que nos desplazamos hacia la derecha por un período, y aumenta dentro de un grupo, hacia abajo. Según esto podemos distinguir tres familias: metales, no metales y semimetales.
A18.- Los elementos metales se agrupan en las familias 1 al 12 en los grupos alcalinos, alcalino-térreos y metales de transición. Indica los principales elementos de estos grupos.
A19.- Los elementos no metales están en los grupos del 14 al 18. Indica los nombres de estos grupos y sus principales elementos?
A20.- Hay un grupo de elementos semimetales o metaloides, que están en los grupos 13 al 17, en medio de metales y no metales. ¿Cuáles son estos elementos?
A21.- ¿En qué lado de la Tabla Periódica es más acentuado el carácter metálico: derecho o izquierdo? ¿Y quién tendrá carácter más metálico, el potasio o el cinc?
A22.- Resume las características de cada familia, metales, no metales y semimetales.
A23.- Consulta la tabla periódica y clasifica los siguientes elementos en metales, no metales y semimetales: bario, yodo, cobalto, nitrógeno, hierro, hidrógeno, germanio, plomo, cromo, bromo, arsénico, azufre, rubidio, cadmio y uranio.
A24.- Los elementos artificiales son los de número atómico 43, 61 y 93 en adelante. Localiza en la tabla periódica los elementos 43, 61, 93, 94, 95. 103 y 106 e indica sus nombres y símbolos.