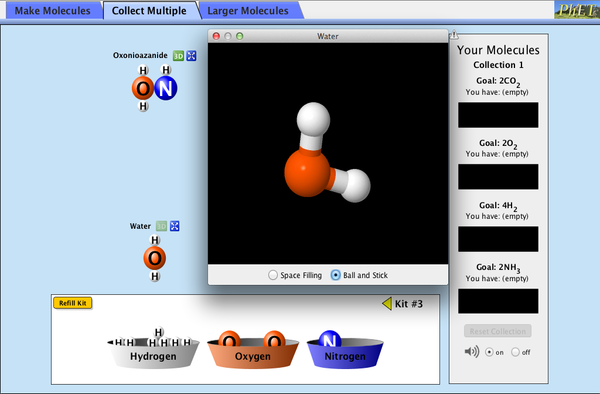
DOCUMENTACIÓN.- En el libro de texto, lee las páginas75-76-77-78 y 79
Ya sabes qué es una REACCIÓN QUÍMICA. La forma en la que escribimos y expresamos una reacción química se llama ecuación química. En ella se describen las sustancias con sus respectivas fórmulas, siendo habitual indicar el estado de agregación, sólido (s), líquido (l), gaseoso (g) o en disolución acuosa (ac). Ahora vas a aprender:
- Una reacción puede emitir o absorber energía (calor).
- Las ecuaciones químicas deben estar AJUSTADAS, utilizando coeficientes estequiométricos.
- En una reacción química se cumple la ley de conservación de la masa.
HAZ
LAS SIGUIENTES ACTIVIDADES:
A6.-
Experimental:
Una reacción que enfría. La
reacción entre el hidróxido de bario y el nitrato de amonio es
endotérmica.
Realizamos la experiencia y describimos lo que observamos. Se trata
de la siguiente reacción: Ba(OH)2
+ 2 NH4NO3
→
Ba(NO3)2
+ 2 NH3
+ 2 H2O
A7.-
Las reacciones químicas, para que estén bien formuladas, deben
representarse mediante una ecuación química. Por ejemplo, la
reacción de formación del agua sería:
H2
(g) + O2
(g) →
H2O
Pero falta algo, hay que ajustar. Esto quiere decir, igualar el
número de átomos: 2
H2
(g) + O2
(g) →
2 H2O.
Los números, antes de las sustancias, son los coeficientes
estequiométricos, e indican el número de moléculas (si no hay
ningún número, es el 1). Ajusta las siguientes reacciones químicas:
a)
Mg (s) + O2
(g) →
MgO (s) b) Fe (s) + O2
(g) →
Fe2O3
(s)
c)
Ca (s) + O2
(g) →
CaO (s) d) Mg (s) + HCl (ac) →
MgCl2
(ac) + H2
(g)
e)
NH4NO2
(s) →
N2
(g) + H2O
(l) f) H2CO3
(s) →
CO 2
(g)
+ H2O
(l)
A8.-
¿Qué dice la ley de conservación de la masa?
A9.-
Aplicamos
la ley de conservación de la masa a la siguiente reacción:
CH4
+ 2 O2
→
CO2
+ 2 H2O.
Si usamos las masas moleculares, tendremos
16
u + 2·32 u →
44 u + 2·18 u Comprueba que masa (reactivos) = masa (productos)
Si
aplicamos las masas moleculares en gramos (las mismas cantidades, que
representan MOL)
16
g + 2·32 g →
44 g + 2·18 g También nos sale masa (reactivos) = masa (productos)
= 80 g
Si
la entiendes sabrás resolver la siguiente tabla: CH4
+ 2 O2
→
CO2
+ 2 H2O
¿?….
224 g 154 g 126 g
A10.-
Comprobación experimental
 de
la ley de conservación de la masa. Este
experimento lo puedes hacer en casa: ponemos un poco de bicarbonato
de sodio (NaHCO3)
en un globo y algo de vinagre en una botella o matraz. Sin que caiga
el bicarbonato, cerramos la boca de la botella con el globo y lo
pesamos. Luego levantamos el globo y dejamos caer todo el bicarbonato
y veremos como se hincha el globo. Comprobamos la masa, cuando
termine la reacción.
de
la ley de conservación de la masa. Este
experimento lo puedes hacer en casa: ponemos un poco de bicarbonato
de sodio (NaHCO3)
en un globo y algo de vinagre en una botella o matraz. Sin que caiga
el bicarbonato, cerramos la boca de la botella con el globo y lo
pesamos. Luego levantamos el globo y dejamos caer todo el bicarbonato
y veremos como se hincha el globo. Comprobamos la masa, cuando
termine la reacción.
a)
Copara las masas y razona qué hubiera sucedido si no estuviese el
globo. ¿Por qué se hincha el globo.
b)
¿Qué ha sucedido? Para explicarlo, hay que usar ecuaciones químicas
NaHCO3
(s) + CH3COOH
(ac) →
CH3COONa
(ac) + CO2
(g) + H2O
(l)